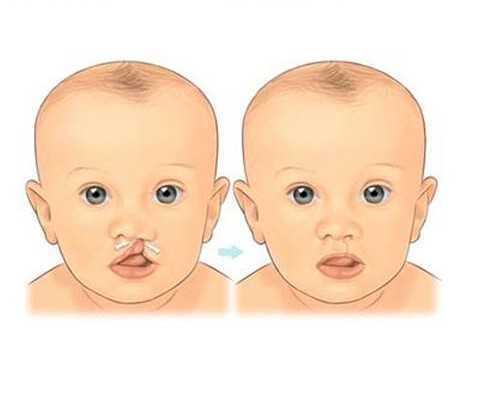
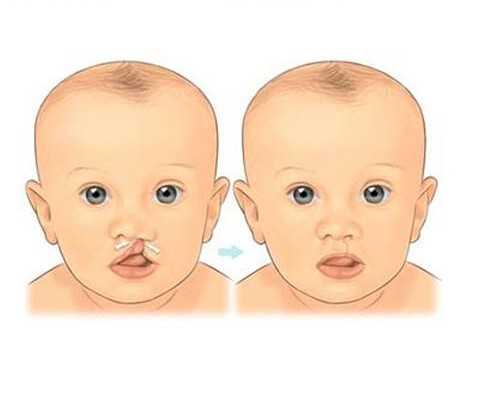
試管嬰兒干細胞移植技術是第四代試管嬰兒嗎?
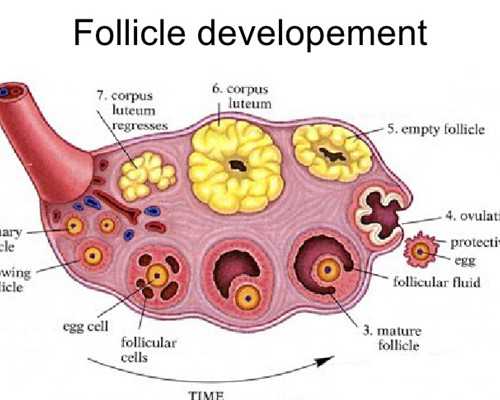
試管嬰兒干細胞移植技術就是卵子干細胞線粒體移植技術,也可以稱之為第四代試管嬰兒技術,該技術就是提取卵子干細胞(EggPCSM)中產生能量的線粒體,然后注射到其他成熟的卵子中,恢復老化卵細胞的活力,通過改善能量水平來提升卵細胞的健康狀態,然后這類卵細胞體外受精的成功率就得到了大大提升。
試管嬰兒卵子干細胞技術依據的原理就是獲取女性自身的卵巢干細胞,提取出其中的線粒體,并將這些線粒體注射到她自身的卵細胞,以提高卵細胞的質量。2015年世界上首例“干細胞嬰兒”,也被稱為“第四代試管嬰兒”就是通過此技術誕生的。
尿毒癥現狀
據流行病學調查,我國慢性腎臟病的患病率為10.8%,現患者人數已超過一億。
預測到2040年,慢性腎臟病將成為全球第五位的致死病因,而慢性腎病的進一步發展結果就是尿毒癥!!!
干細胞治療尿毒癥有著天然的優勢,今天咱們就針對尿毒癥的傳統療法與干細胞療法進行全面分析,更直觀地將干細胞療法的優勢呈現出來!
什么是尿毒癥
尿毒癥,簡單來說就是腎臟功能衰竭,無法將人體內的代謝產物、廢物、尿素和多余的水分等排出體外,導致人“中毒”的一系列綜合癥。
慢性腎臟病是一個長期持續進展的過程,共分為5個時期。前3個時期中,腎臟的代償作用可以基本完成腎臟的功能,病人通常沒什么不舒服。
而到了第4期,腎功能的損害進入不可逆的階段,病人的食欲減退、貧血、血鉀高、消化道出血等癥狀日漸明顯,甚至心臟等其他器官也開始衰竭。
當慢性腎臟病進展到終末期,就是我們常說的“尿毒癥”了。
尿毒癥現有治療方式的局限性
目前,治療尿毒癥主要就是“三板斧”:血液透析、腹膜透析和腎移植。
血液透析(腎透析的缺點):
每次需要扎針;貧血比較嚴重;透析前后血壓會受影響,對心血管疾病和糖尿病病人較不利;無法任意更改透析時間;感染乙型肝炎和丙型肝炎的風險大大增加;透析費一年大約需要6萬元左右。
腹膜透析的缺點
在腹腔內置入腹透管,操作不當容易感染,每年需要4-5萬元。
腎移植的缺點
供體的缺乏:目前全國每年接受腎移植者僅有5000多例,大約每150個等待的患者,只有一人可能得到腎移植的機會。
一次腎移植手術,在我國大約需要30-60萬元,對于普通家庭來說,這是一個沉重的經濟負擔。
血液透析、腹膜透析、腎移植的種種局限性,給尿毒癥患者的經濟條件與身體狀況都造成了影響。
而干細胞療法的出現為尿毒癥患者帶來了曙光,有望告別透析和腎移植。
干細胞在尿毒癥治療中的探索
對于一種全新的療法,首先要搞清楚的就是其作用機理。
基于此,科學家們通過反復的實驗,發現干細胞在修復腎臟損傷、保護腎臟功能和結構從而延長動物存活方面具有治療潛力。
其中,間充質干細胞(MSCs)是最常用的一種,其很容易在實驗室中擴增,產生大量的治療劑量;此外,間充質干細胞不表達血型、DR抗原和共刺激分子等,免疫原性低,使得使用同種異體細胞成為可能。
MSCs主要通過以下機制發揮作用
MSCs轉分化為腎臟特異性細胞以重新填充腎臟受損缺失細胞。
MSCs的旁分泌效應:分泌大量的細胞因子、趨化因子和生長因子,包括IL-6和IL-11、血管內皮生長因子(VEGF)、粒細胞集落刺激因子(G-CSF)等,以及外泌體,促進上皮細胞增殖和血管生成。
刺激腎細胞分泌促紅素。而促紅素可以促使紅細胞的生成,緩解機體貧血的狀況。
另外,干細胞通過細胞間的相互作用及產生細胞因子而抑制T細胞的增殖及其免疫反應,從而發揮免疫重建的功能,減少腎臟移植后的免疫排斥反應。
干細胞治療尿毒癥臨床案例
干細胞療法主要有三種形式:干細胞移植治療、干細胞輔助腎移植、3D打印腎移植。
干細胞移植治療
Cantaluppi等人總結了Clinical Trials.gov干細胞治療各種腎病的Ⅰ/Ⅱ期臨床試驗,大部分探究目的是確定干細胞治療的安全性和有效性。
Packham DK等人開展一項Ⅰ期臨床試驗,納入30例糖尿病腎病患者,靜脈注射干細胞,并隨訪60周。結果發現,干細胞輸注安全且耐受性良好,患者各項腎臟指標有所改善。
2011年國內發表的文獻顯示,研究人員對一名24歲的男性尿毒癥患者進行了兩次干細胞移植。
患者干細胞移植前尿素氮26.54 mmol/L、肌酐 826.9μmol/L。干細胞移植后兩次復查患者血常規及腎功能,報告顯示患者抗基底膜抗體由陽性轉陰性,尿素氮、肌酐等指標均下降,表明干細胞療法對患者腎臟的修復起到了很好的作用。
干細胞輔助腎移植
2020年,一篇發表在《干細胞移植醫學雜志》的文章表明:活體腎移植在間充質干細胞輸注后可停用維持性抗排斥藥物,移植器官能夠長期存活,不發生器官排異反應!
2010年,意大利的幾位科學家們將基礎研究的成果應用于人體實驗。一位37歲,接受了親屬活體腎移植的男性,參與了這項研究。

在移植后的六天內,每天靜脈接受低劑量的兔抗人胸腺細胞免疫球蛋白輸注治療,作為輔助。
在移植后第2年,患者開始逐漸減少免疫抑制劑,一共用了5年多的時間完全停了所有的藥物。
3D打印腎移植
2018年2月8日,一項具有突破性進展的研究成果刊登在著名學術期刊《干細胞報告》上。
曼徹斯特大學的研究團隊將人類胚胎干細胞培養成腎小球,然后將腎小球與類似結締組織的凝膠物混合后注入到實驗小鼠真皮下。
三個月后,腎臟的基本單位—近端腎小管、遠端腎小管、腎小球囊和亨利氏套等在小鼠體內形成。
該項目負責人、曼徹斯特大學Susan Kimber教授說,如果這個過程可以被完善和擴大的話,它也可以用來生長整個移植器官。
這一研究引起了全球轟動,這或將成為腎病治療史上一個重要的里程碑,尤其是近年來3D打印技術的興起,人工腎移植或許會加速到來。
干細胞技術,作為一門先進的醫學技術,不僅為一些疑難雜癥的干預帶來了希望,也勢必引領新的醫療革命。解決患者疼痛困擾,造福人類。
來源:干細胞之父公眾號